Возбуждение, эмиссия, и эффективность
Многие материалы флуоресцируют слабо, поэтому когда биологи говорят о флуоресценции, они обычно говорят о флуоресценции конкретной молекулы, превращающей большую часть поглощённого света в свет других длин волн. Молекулу такого рода часто называют «флуорофором». Независимо от количества преобразуемого света, флуоресценция любой молекулы описывается тремя свойствами. Первое – спектр возбуждения (рис. 7.2).
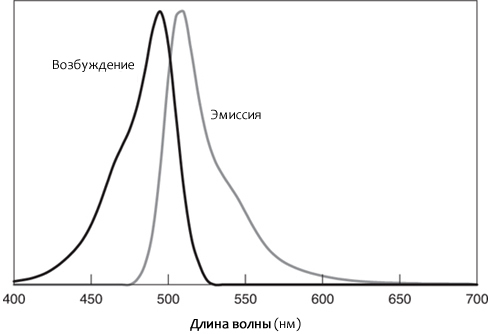
Хотя и под другим именем, по существу мы говорим о спектре поглощения молекулы. Разумеется, фотон должен поглотиться, прежде чем возбудить флуоресценцию. Существуют длины волн света, которые поглощаются, но не способствуют флуоресценции (например, с очень высокими или низкими энергиями), но в ближнем УФ/видимом диапазоне для биологических молекул спектры поглощения и возбуждения почти идентичны. Как и в случае с зрительными пигментами, после поглощения фотона его энергия обычно не влияет на то сколько, или на каких длинах волн излучается света. Вместо этого, как и с зрительными пигментами, длина волны падающего света влияет только на вероятность того, что фотон будет поглощён, и произойдёт флуоресценция. Этот факт, известный как «Правило Каши», может показаться немного странным, так можно предполагать, что энергия поглощенного фотона должна оказывать большее влияние на вероятность его возвращения. Это правило основано на том факте, что флуоресценция почти всегда происходит во время последнего прыжка между наименьшим возможным возбужденным состоянием и основным энергетическим состоянием. Таким образом, пока существует достаточно энергии, чтобы находится выше этого первого возбужденного состояния, флуоресценция не произойдёт. Правило не является абсолютным, однако оно из категории правил, наблюдаемых на практике.
Второе определяющее свойство флуоресцентной молекулы – её спектр эмиссии. Можно заметить, что не все испускаемые фотоны имеют одну и ту же длину волны, хотя должны были бы, если исходить из положения о последнем прыжке между самым низким возбужденным состоянием и основным состоянием. Это связано с добавлением и вычитанием вибрационных энергий и другими прибамбасами, дающими намёк на истинную сложность происходящих процессов. Спектр эмиссии по существу означает только вероятность того, что излучаемый фотон будет иметь определенную длину волны. Вы заметите, что спектры возбуждения и эмиссии выглядят как слегка перекрывающиеся зеркальные изображения друг друга. Это характерно для многих флуоресцентных молекул, но не является универсальным правилом.
Наконец, последним свойством флуоресцентной молекулы является эффективность. Её определение можно дать двумя способами: количество эмитированной энергии, делённое на количество поглощённой энергии, или количество эмитированных фотонов, делённых на количество поглощённых фотонов. Последний способ также называется «квантовым выходом». Я лично считаю квантовый выход немного странным, так как он теоретически позволяет вам получить более 100% от поглощённых фотонов. Однако квантовая эффективность является общепринятым термином и для биологов имеет смысл, поскольку зачастую их больше заботит количество фотонов, чем общий объём энергии.
Важно отметить, что при определении эффективности флуоресценции играет роль количество поглощённых флуорофором, а не количество падающих на него фотонов. Поэтому эффективность не получится посчитать, просто измерив входящий световой поток, и разделив его на исходящий световой поток. Необходимо знать, какая часть света фактически была поглощена. Это также означает, что что-то может иметь высокую эффективность флуоресценции, но флуоресцировать слабо, если вещество поглощает мало света. Это ещё один из тех случаев, когда нужно быть внимательным. Например, аналогично звучащий термин «квантовая эффективность» имеет в своем знаменателе количество падающих (а не поглощенных) фотонов.
Итак, учитывая эти три свойства, как на самом деле рассчитываете, какова эмиссия света на каждой длине волны? Из-за возрастающего числа исследований животной флуоресценции и её возможного экологического значения, полезно знать, как это сделать. Поэтому я подробно рассмотрю этот вопрос. Во-первых, необходимо рассчитать, сколько света поглощено. Предположим, у вас есть участок флуоресцентных молекул на предметном стекле микроскопа. Молекулы имеют молярную объемную плотность ρ, а участок имеет толщину t. Вы освещаете этот участок сверху светом широкого спектра, что приводит к облучённости E(λ). Используя уравнения поглощения из главы 4, количество поглощенных на каждой длине волны фотонов:
7.1
Спектральная поглощательная способность A(λ) по обыкновению даётся в единицах оптической плотности (то есть, используя десятичные вместо натуральных логарифмов). Подобно поглощательной способности зрительных пигментов, она обычно также делится на две части: (1) спектр, нормализованный по пику одной длины волны, и (2) коэффициент. В этом случае нормализованный спектр – это так называемый «спектр возбуждения/поглощения Vex(λ)», а коэффициент обычно указывается как молярный коэффициент поглощения M (другими словами A [λ] = MVex[λ]). Это означает, что плотность ρ должна быть в молярных выражениях. Так поступать не обязательно, но большинство флуорофоров описывается через их молярный коэффициент поглощения, поэтому так часто бывает проще. Как и при расчете поглощения зрительного пигмента (см. Главу 4), необходимо следить за единицами измерения. Опять же, руководящий принцип должен состоять в том, чтобы возводимые в степень числа были безразмерными. Молярный коэффициент поглощения обычно указывается в Л/мол-1 см-1 Если это соблюдается, то нормально давать концентрацию вашего флуорофора в молярности (моль/л), а его толщину – в см.
Уравнение 7.1 дает только количество света, поглощаемого на одной длине волны, поэтому вам нужно суммировать диапазон длин волн. Эта сумма такова:
7.2
Обычно использование интервалов длины волны шагом 10-нм является достаточным, но, если кривая спектра возбуждения особенно крута, может потребоваться перейти на 5-нм интервалы, чтобы точно отобразить её.
Когда известно общее количество поглощенных фотонов, довольно просто вычислить, сколько света излучается на каждой длине волны. По сути, это только:
7.3
где Q - эффективность флуоресценции, а Vem(λ) – спектр эмиссии.
Нужно иметь в виду то, что при флуоресценции эмиссия происходит одинаково во всех направлениях. Эта особенность флуоресценции имеет экологические последствия, до которых мы скоро доберёмся, но пока нам нужно подумать о том, как рассчитать фактическую энергетическую яркость флуоресцирующего участка. Удобно, что яркость излучающей одинаково во всех направлениях поверхности (известной как «излучатель Ламберта»), хорошо известна, и представляет собой просто количество излучаемых фотонов, деленное на π. В этом случае, поскольку половина фотонов движется в другом направлении (т.е. отправляется в противоположную от поверхности сторону, и уходит от нас), нужно будет разделить на 2. Таким образом, излучаемая яркость Lem(λ) равна Nem(λ)/2π. Используя этот факт и объединяя уравнения 7.2 и 7.3, получаем:
7.4
Уравнение может выглядеть немного тяжеловесно, но его просто решить в программе для работы с электронными таблицами или в скрипте MatLab. Однако, как и в случае поглощения света визуальными пигментами, нужно работать медленно и быть внимательным с единицами измерения.

